-
新闻
固定床反应器全封闭生产工艺:外泌体安全性再上新台阶
发布日期:2026-05-08
近年来,间充质干细胞来源的外泌体在再生医学与疾病治疗领域展现出巨大潜力。就在今年4月13日,国内首个外泌体I类新药STX11101注射液获CDE受理,标志着我国外泌体药物研发从实验室阶段正式跨入临床转化的新纪元。然而,传统2D培养及分批式纯化工艺存在批间差异大、污染风险高、可扩展性差等问题。本文以人脐带来源间充质干细胞(hUC-MSCs)采用化学限定培养基3D培养及分批补料(fed-batch)收获工艺为例,探索了CEL-G® Culture Ad60固定床生物反应器(Ad60 FBR)与CEL-G® TFF Lab系列外泌体浓缩系统(TFF Lab)在线偶联的全封闭工艺流程。该工艺实现了从细胞培养到外泌体收获及浓缩纯化的一站式、连续化、标准化操作,显著提升了外泌体的纯度、安全性及生产效率,为“药品级”外泌体生产工艺的建立提供了可行路径。
干细胞外泌体作为无细胞治疗制剂,具备低免疫原性、易于储存和运输等优势,已成为再生医学研究的热点。外泌体工艺的目标是在符合cGMP的条件下,获得高产量、高质量、一致性的外泌体。外泌体的生产始于细胞,其产量与质量高度依赖培养条件;下游纯化的核心挑战在于平衡纯度、回收率与生物活性。然而传统生产模式大多采用2D培养与多级纯化步骤,存在操作开放、批次稳定性差、外源性污染风险高等问题。为满足临床级外泌体的生产要求,亟需构建一套封闭化、自动化、连续化的生产工艺体系。
本案例采用化学限定培养基将脐带来源的间充质干细胞(hUC-MSCs)通过Ad60 FBR的3D培养和在线偶联方式衔接下游TFF Lab外泌体浓缩系统,实现外泌体的高效制备。

图1. 同腾新创CEL-G®外泌体一体化制备平台
-
培养体系:固定床膜面积为3.6 m2,接种密度为1.68×104 cells/cm2(P6代),培养体积从2.5 L起始,通过分批补料策略扩大至10 L。
-
培养条件:pH 7.0±0.1,温度37.0℃,DO 25%。
-
培养基:采用化学成分明确、无动物源成分的CEL-G® Culture MSC Standard CD培养基,支持MSCs连续扩增11代,避免外源性污染。
-
补料策略:在Day 3和Day 6等体积补充培养基,Day 9收获10 L上清液。
-
CelGrid™️ 微型固定床生物反应器对照组:固定床膜面积为0.3 m2(分别采用P4代和P6代细胞接种)。

图2. 同腾新创CelGrid™微型固定床生物反应器和CEL-G®系列固定床生物反应器
-
处理流程:上清原液 → 澄清 → 浓缩 → 缓冲液置换 →除菌收获 → 外泌体浓缩液。
-
关键技术:TFF Lab系统,采用生理盐水进行缓冲液置换,总处理时间小于1小时,终体积浓缩25倍。
-
处理能力:单批次处理10 L上清液,收获外泌体浓缩液400 mL。
在细胞接种后每天取样进行葡萄糖、乳酸及LDH的相关代谢指标检测。统计结果显示,无论是对于不同细胞代次的FB-0.3还是放大到FB-3.6,细胞代谢趋势均较为一致,并且代谢均较为活跃。于Day1、3、6、9进行取样条活死细胞荧光染色观察,细胞均呈多细胞聚集球状生长,表现出较强的绿色荧光(Calcein-AM 活细胞)且未观察到红色荧光(PI死细胞)。同时,分别于Day3、6、9取上清进行NTA检测,检测结果对于FB-0.3(P4代和P6代)和FB-3.6趋势一致,其中FB-0.3(P4代)NTA颗粒浓度最高,提示低细胞代次有利于收获更高的产量。FB-3.6收获10L细胞上清液,颗粒浓度达7.5×109 Particles/mL,总颗粒数达7.5×1013 Particles。生化代谢结果、荧光染色观察结果及NTA检测结果均证明细胞生长状态良好。具体生化代谢浓度统计数据对比、取样条荧光染色照片及NTA检测结果如下:
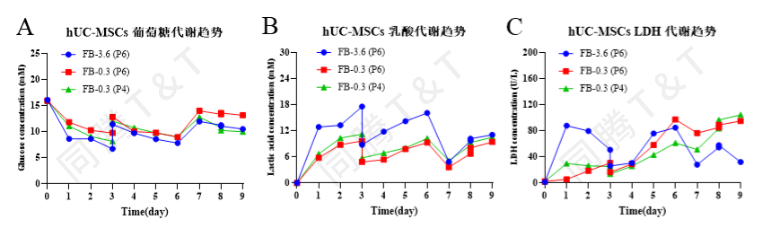
图3. hUC-MSCs在CelGrid™ FB-0.3及Ad60 FB-3.6 上培养后生化代谢浓度对比曲线:(A)葡萄糖代谢趋势; (B)乳酸代谢趋势; (C)LDH 代谢趋势
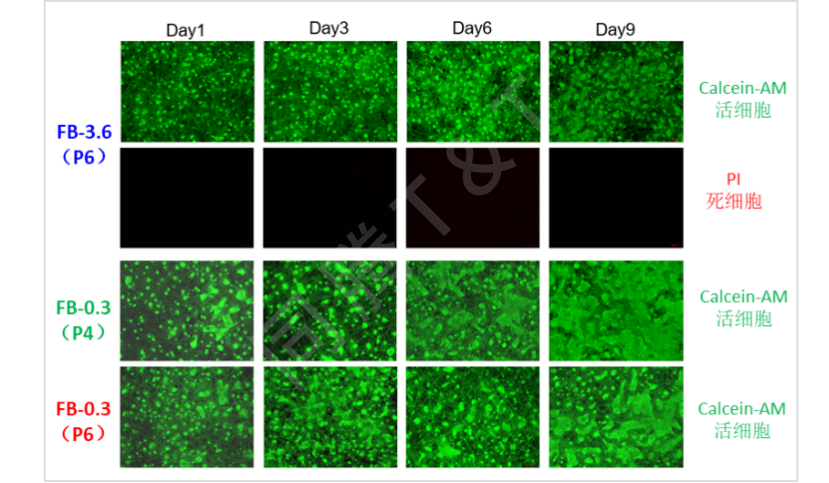
图4. hUC-MSCs在CelGrid™ FB-0.3及Ad60 FB-3.6 上培养后于不同天数取样条活死细胞荧光染色照片
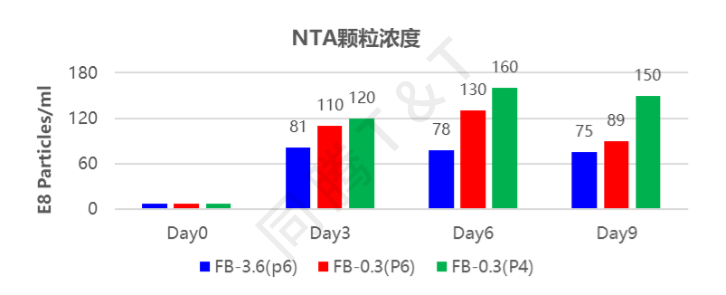
图5. hUC-MSCs在CelGrid™️ FB-0.3及Ad60 FB-3.6 上培养后于不同天数上清液中NTA颗粒浓度
补料阶段,于Day3补充2.5L新鲜培养基,Day6补充5L新鲜培养基,Day9 进行细胞上清原液(共10L)的全收获。同时,在线偶联下游TFF Lab进行外泌体浓缩纯化。最终收获约400 mL外泌体浓缩液,颗粒浓度达6.5×1010 Particles/mL,蛋白去除率99.5%,颗粒蛋白比达到5.15×108 Particles/μg,且经TEM、WB检测结果证明收获的外泌体均符合团体检定标准。具体外泌体检测数据如下:
表1. hUC-MSCs 3D培养上清原液和外泌体浓缩液检测结果
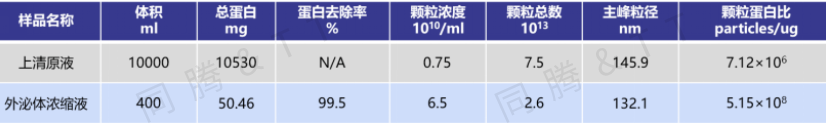
表2. hUC-MSCs外泌体浓缩液无菌、支原体及内毒素检测结果
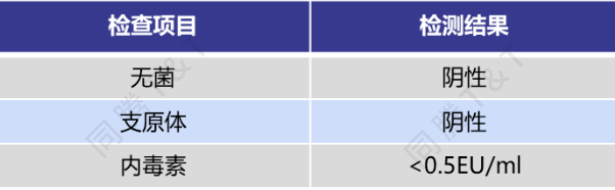
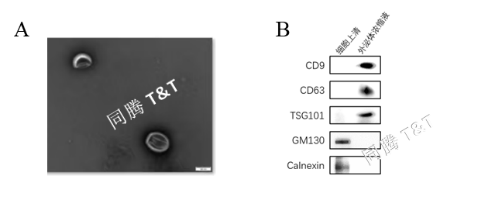
图6. hUC-MSCs外泌体浓缩液 (A) TEM;(B) WB 检测结果
该工艺在多个层面保障了生产过程与产品的安全性:
-
全封闭操作:细胞培养与下游纯化在线偶联,避免开放操作带来的微生物污染风险,提高批间一致性。
-
化学成分明确:培养基无动物源、无人源成分,杜绝外源性病原体或免疫原性物质引入,同时也排除了体系中外泌体的干扰,确保实验结果的准确性。
-
质量控制完备:外泌体浓缩液经无菌、支原体、内毒素检测,符合药品级标准。
-
高效去除杂蛋白:杂蛋白去除率>99.5%,颗粒蛋白比>5×108 Particles/μg,外泌体特异性标记物阳性率高。
该工艺实现了从细胞培养到外泌体提取的一站式完整解决方案(Standard CD培养基 + Ad60 FBR + TFF Lab),具有以下重要意义:
-
标准化与规模化:固定床培养结合分批补料策略,支持高密度细胞培养和高效外泌体分泌,单批次可稳定收获10 L上清,具备良好的放大潜力。
-
连续化生产:在线偶联下游纯化系统,避免中间多批次收获液的冻融合并环节,缩短工艺路径,提升生产效率。
-
药品级生产工艺:全封闭、无动物源、高纯度、高回收率的设计理念,符合GMP导向,为外泌体药物开发奠定工艺基础。
-
广泛适用性:该平台可推广至其他类型干细胞或细胞源外泌体的生产,助力再生医学与细胞治疗领域的发展。
本研究展示的固定床生物反应器在线偶联外泌体浓缩纯化系统,构建了一条高效、安全、可扩展的全封闭外泌体生产工艺。该工艺在纯度、安全性、批间一致性等方面均表现优异,为干细胞外泌体的临床应用转化提供了坚实的工艺支撑。
- 021-50826962
- sales@ttbiotech.com
-
江苏省苏州市太仓市昭溪路90号
