-
新闻
固定床生物反应器:iMSC 3D培养与外泌体规模化生产的稳健之选
发布日期:2025-08-15
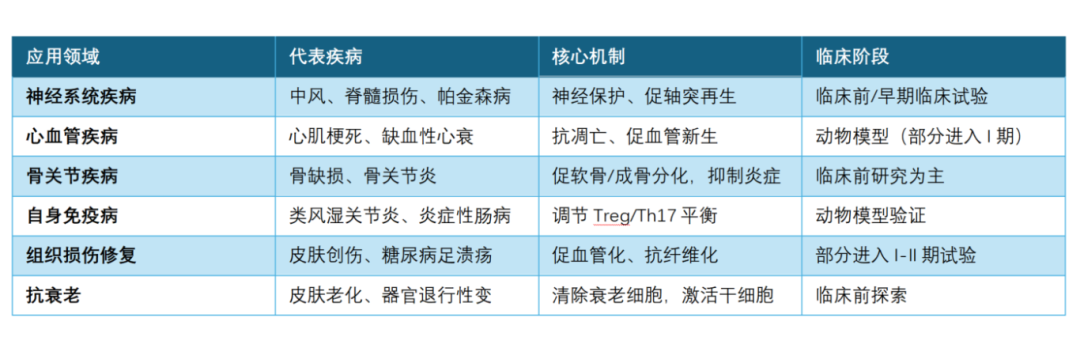
iPSC来源的MSC外泌体(iPSC-MSC-Exosomes,iMSC-Exos)的研究,是再生医学和细胞治疗领域的热点方向,近年来取得了显著进展,并展现出巨大的临床应用潜力。
iPSC可无限扩增,解决了传统MSC外泌体来源受限(如供体差异、衰老、批次不稳定)的问题。
通过标准化诱导分化流程,可获得均一性高的MSC样细胞,提升外泌体生产的稳定性。
规避了iPSC直接应用的致瘤风险,外泌体本身无增殖能力,安全性更优。
目前,iMSC-Exos的研究大多停留在实验室阶段,大规模稳定生产高质量外泌体仍是主要障碍,需建立GMP级生产流程。
iPSC 来源的外泌体需严格表征以确保无残留多能细胞,同时需解决批次间一致性问题和确保供体筛查及表征的安全性。
iMSC的规模化培养与扩增需要优化细胞培养条件(如溶解氧、pH值、处理时间)及反应器设计,确保从实验室到产业化规模的可扩展性和稳定性。 但目前报道的一些3D培养系统(如水凝胶、微载体或中空纤维生物反应器)虽有望提高产量,但存在微载体残留污染等问题,为下游纯化分离带来挑战。
同腾新创推出的CEL-G® Culture Ad60固定床生物反应器(Ad60 FBR)是一款规整式固定床生物反应器,主要用于贴壁细胞的培养及产物收集,适用于病毒疫苗,细胞和基因治疗,外泌体生产等领域。规整式FBR 是目前可用于培养贴壁细胞的最具放大性的技术,其独特的瀑布流设计能完成高效的气质传递、可为细胞生长提供低剪切力的3D培养环境。

图1. 同腾新创Ad60 FBR和规整式固定床结构
与微载体3D培养相比,Ad60 FBR固定床系统在规模化、细胞稳定性、下游处理简化等方面具备明显优势。
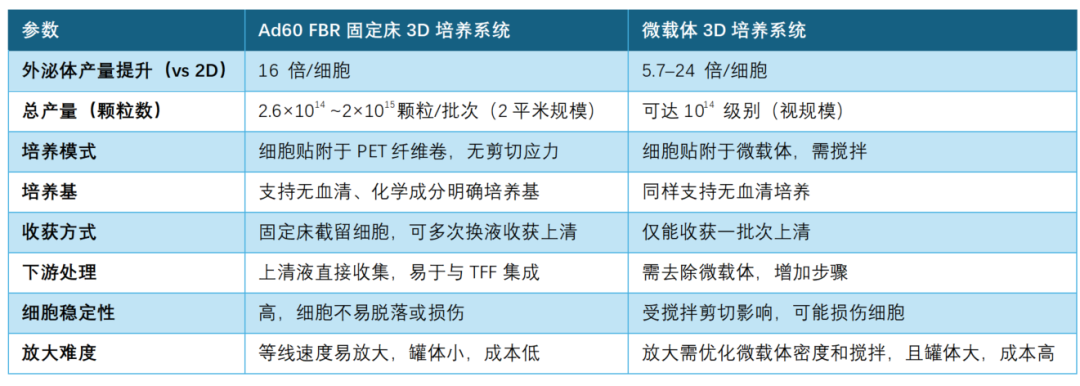
固定床膜材具有细胞固定和截留作用,不仅可通过更换循环瓶培养基实现多次收获上清,且产生的上清无杂质污染,是临床级、规模化、无血清iMSC-Exos制备的理想选择,以下将介绍两个采用Ad60 FBR制备iMSC-Exos的研究案例。

图2. iMSC在2D和3D (Ad60 FBR 2m2) 培养中工艺概述及工艺流程
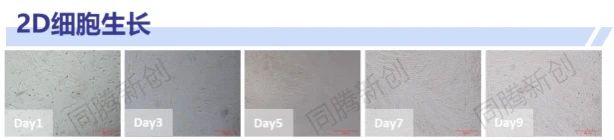
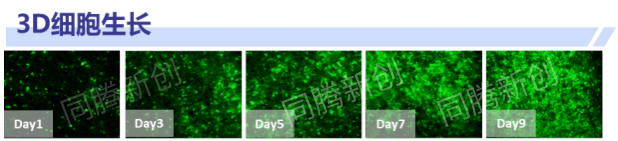
图3. iMSC的2D及3D细胞生长状态
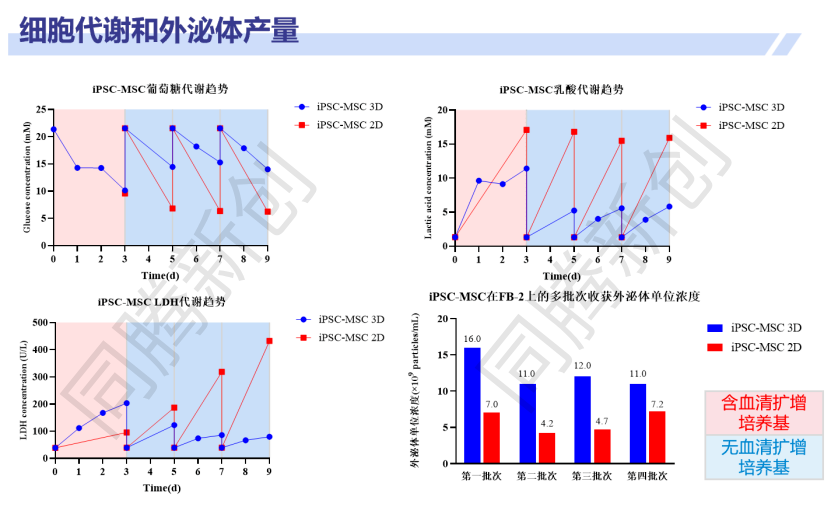
图4. iMSC在2D和3D (Ad60 FBR 2m2) 培养中细胞代谢情况及外泌体产量对比
研究结论:iMSC在固定床中贴附较快,且在无血清条件下仍能快速扩增(图3),不同培养基中3D培养上清中外泌体颗粒浓度均较2D培养显著提高,且3D培养条件下细胞代谢更稳定,固定床中细胞LDH释放水平更低表明细胞活率更高(图4)。
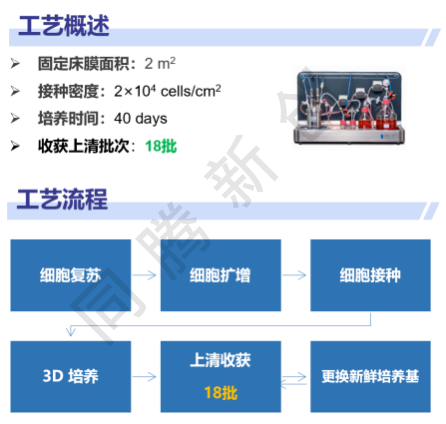
图5. iMSC在Ad60 FBR 2m2中连续培养工艺概述及工艺流程
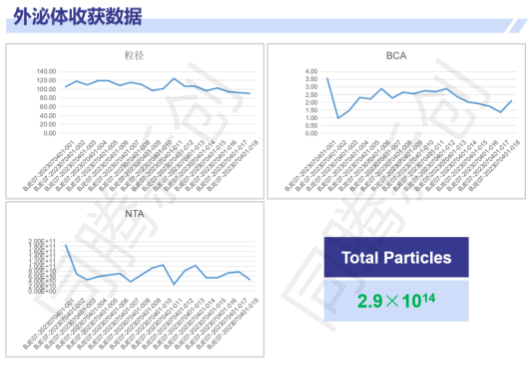
图6. iMSC在Ad60 FBR 2m2中连续培养外泌体收获数据(粒径、BCA及NTA)
研究结论:在这个案例中iMSC在固定床中可以连续无血清培养长达40天,共收获18批上清液,总产量达到2.9×1014 particles,为同体量细胞工厂的20-30倍!
固定床生物反应器在iMSC的3D培养中不仅可行,而且收获的外泌体在产量、质量和工艺可控性上优于微载体系统,特别适合临床级、规模化、无血清外泌体制备。如需进一步放大至GMP级别生产,建议采用Ad60固定床上游细胞培养+切向流过滤(TFF)下游浓缩超滤组合工艺,以实现高效率、低剪切、低污染的连续生产体系,进而推动iMSC-Exos从实验室走向临床转化。
- 021-50826962
- sales@ttbiotech.com
-
江苏省苏州市太仓市昭溪路90号
